姚要兵医生的科普号
- 精选 MOG抗体阳性与视神经脊髓炎谱系疾病的关系
女性比男性更易患病 本研究中,女性患病数量是男性的2.8倍。在AQP4抗体阳性的NMOSD中,女性的性别是独立的危险因素[83,84]。后来我们发现了白人患者中女性数量更多,男女比例为9:1[34]。目前和之前的群体中,MOG抗体阳性患者中的女性比例与AQP4抗体阴性的NMOSD[34]和典型的MS[84]相似。最终随访中女性较高的EDSS中位分数提示女性可能受到疾病的影响更重,即便疾病持续时间相对较短。但是我们需要验证性的研究来证实这一发现。 疾病发作可能发生在孕期或产后 目前还没有系统的研究过怀孕对MOG抗体阳性EM的影响。最近一项研究显示,怀孕可能对NMO的疾病进程产生不良影响;但是,没有数据表明怀孕对患者的AQP4抗体 或 MOG抗体状态有何影响。研究者们发现,在怀孕之后的第一个月发病率明显升高,生产后一年会发生更严重的残疾。在另一群体中,14/40 AQP4抗体阳性的患者都是在孕期(n =3)或生产/流产后1年内(n =11)出现了NMOSD的首次发作。虽然孕期和孕前的ARR并无差异,但是在产后第一个月和第二个月内,ARR显著升高;而且,77%的生产行为都与产后复发相关。在MS中,怀孕被认为可以减少复发,尤其是在第二个月和第三个月内;虽然复发率在产后的3-6个月会升高,但不会增加长期致残率。在目前的研究人群中,大约四分之一的MOG抗体阳性的女性在怀孕期间后产后都至少经历了一次复发。更重要的是,有三位患者在产后首次发病。这可能表明,怀孕和或生产相关的免疫改变在诱导发作和疾病感应可能起到了一定的作用。但是,我们已知大多数发作和整个女性亚组的患病情况与怀孕和生产无关,其他的危险因素可能更为重要。以这些数据为基础,我们需要系统性的前瞻性研究来证明怀孕和生产在MOG抗体阳性EM中发挥的作用。 感染及疫苗接种后的发作 40%的患者至少在一次发作之前存在感染,至少11例患者在感染后短期内发病,2例患者在疫苗接种后短期内发病。这同样发生在AQP4抗体阳性的NMOSD中,据报道,20-30%的案例在发病前经历过感染。急性感染也被认为是导致典型MS临床发作的诱因。但是,感染或疫苗接种与MOG抗体阳性EM之间的确切关系依旧尚未可知。虽然没有分子模拟的证据,我们依旧可以推测出,感染相关的免疫改变和或血脑屏障的损伤导致了中枢神经系统病变的发生。AQP4抗体阳性的NMOSD中,急性发作确实与上升的QA1b相关,QA1b的升高,则与结构性屏障损伤相关。根据目前的研究结果,在MOG抗体阳性的患者中大约三分之一都存在QAlb的升高。QAlb也反映了脑脊液流速的变化。2例免疫接种后发病的案例均发生在接种破伤风、白喉和百日咳疫苗后,这值得更深入的研究。根据记载,两位患者都发展为进展性病程。这与传统的免疫接种后ADEM不同,免疫接种后ADEM通常是单相病程。 脑脊液结果与MS不同,但与AQP4抗体阳性的NMO相似 脑脊液的检查很有希望被用于鉴别典型的MS和MOG抗体阳性的EM,但不能用于鉴别MOG抗体阳性的EM和AQP4抗体阳性的EM:因为在AQP4抗体阳性的患者中,OCB和阳性的脑脊液/血清IgG比例在大多数MS患者中均存在并且被当做MS的诊断标志,但90%的MOG抗体阳性患者却不具备此项特征。而且,在仅有的6位OCB阳性的患者中,有2位患者的OCB后来消失了;与此相反,MS患者在几十年后OCB水平依旧很稳定。64 % AQP4抗体阳性的NMO患者至少一次在脑脊液中找到了中性粒细胞,但典型的MS无此特征。 OCB的缺乏以及脑脊液粒细胞的异常增多提示临床医生诊断为可疑MS的患者可能是MOG抗体或AQP4抗体阳性的脑脊髓炎。 疾病播散的亚临床证据 我们至少在3位无视神经炎临床表现的患者身上发现了视神经损伤的电生理学证据,在至少在三位无脊髓炎临床表现的患者身上发现了脊髓损伤的电生理学证据。与此相似,我们在21位患者中发现,他们仅患有视神经炎和或脊髓炎而从未有过脑炎或小脑炎的临床表现,却在核磁中发现了幕上的、脑干或小脑的病灶。同时,2位视神经炎患者从未出现过脊髓炎症状,却在脊髓核磁中发现了病灶。这表明,某些案例中可能存在亚临床炎性损伤,我们应该完善核磁和电生理学检查来明确MOG抗体阳性患者中枢神经系统炎症的波及范围。如果我们不仅把临床发作纳入考虑,同时还能通过电生理检查和核磁检查明确亚临床病灶,根据最终随访,我们就能找到37/50 或者 74 %患者疾病播散的证据,如果仅仅依靠临床表现,我们仅能发现26/50 或52 %。 VEP及SSEP未被纳入1999和2006版的NMO诊断标准,NMO的诊断依靠临床上视神经炎和脊髓炎的发作,2015版的NMOSD诊断标准同样如此。在仅仅表现为独立视神经炎或独立脊髓炎的MOG抗体阳性患者中,关于病理学EP的疾病预兆、诊断和治疗方法方面的潜力,以及核磁发现对疾病播散的预示作用,仍需要系统性的研究。在AQP4抗体阳性的NMOSD患者中,我们也发现了亚临床视神经损伤的证据。 双侧视神经炎和视神经炎与脊髓炎同时发生都是常见的首发症状 根据最后的随访,在经历过视神经炎和脊髓炎的患者中,至少40%的人至少有一次二者同时发作的情况,AQP4抗体阳性的NMO患者同样如此。但是,谈到以视神经炎和脊髓炎同时发作为首发症状,MOG抗体阳性的患者比AQP4抗体阳性的NMOSD患者发生率更高。与此相似,既往患者视神经炎的MOG抗体阳性患者与AQP4抗体阳性的NMOSD患者相比,前者以双侧视神经炎起病的可能性更大。同时起病的视神经炎和脊髓炎以及双侧视神经炎作为首发症状时,是具有诊断价值的,临床医生应该考虑MOG抗体检测。 短节段的脊髓病变不能除外MOG抗体阳性 核磁上脊髓病灶超过3个脊髓节段被认为是AQP4抗体阳性NMOSD标志,但是在典型MS中却不常见。在1999年的NMO诊断标准中,长脊髓节段的病变加上临床脊髓炎表现属于支持性证据。而2006版的诊断标准有三个特征,分别是LETM、视神经炎和脊髓炎。我们在本研究和之前研究中所发现的LETM与MOG抗体之间的关系具有重要的鉴别诊断意义。 但是,两项最近的研究表明,AQP4抗体阳性的NMOSD患者中,高达15%的核磁影像上并没有长节段的脊髓损伤。类似的是,我们的MOG抗体阳性的患者中,有8位的脊髓病灶没有超过2个节段;另外10位患者至少有一次核磁显示非长节段病灶,但在此之前和之后的影像均为长节段病灶。MOG抗体或AQP4抗体阳性的脊髓炎是否表现为短节段病灶是时间问题,同时也受到其他因素影响。如果在发作的超早期或者急性期后很久行核磁检查,脊髓病灶可能仍然是长节段的或已处于恢复阶段。 与AQP4抗体阳性的脊髓炎相似,我们的患者中也有许多人至少一次在核磁中发现了超过一个脊髓节段的病灶和脊髓的水肿。但不同的是,AQP4抗体阳性的脊髓炎患者中,部分会出现脊髓坏死性病灶导致脊髓空洞,但在MOG抗体阳性的患者中却从未发现。 病变可能影响整个视觉通路 虽然MOG抗体阳性的患者中,球后视神经炎是非常常见的,但是当此类患者出现视觉症状时,我们也应该考虑到可能是视觉通路上的其他结构受到了损伤。许多患者有视神经乳头炎的征象,核磁上也会发现视神经前部炎症的证据。然而,部分患者存在视交叉病变和或纵向扩展的视神经炎(LEON,同时影响到了视神经的前部和后部)。之前,无论是LEON还是视交叉病变都被认为是AQP4抗体阳性NMOSD的标志。我们的发现与澳大利亚的一项研究得出的结论是一致的,这项报道:AQP4抗体相关的视神经炎和MOG抗体相关的视神经炎与MS相关视神经炎相比,前两者视神经病变长度更长。某位患者是因为视束病变导致了视力损伤。部分患者存在枕部白质病变。 眼周的对比增强要求我们进行更深入的研究 如图9所示,我们不仅仅能在视神经看到对比增强,也可以在眼周神经鞘和眶周看到此现象。这种影像表现可能将来会用于鉴别诊断,也值得更深入的研究。与此发现一致的是,Kim等人在最新的一项研究中发现,18位MOG抗体阳性的患者中有6位出现了周围神经的强化。鉴于这些案例存在不同的核磁特征,是否出现此种现象可能与疾病和治疗状态相关:至少三分之一不存在眼周强化的核磁是在疾病的缓解期进行的,剩下的患者在进行核磁检查之前接受了高剂量的IVMP治疗。 MOG抗体阳性的患者很少合并其他自身免疫病 AQP4抗体阳性的NMOSD患者中至少三分之一合并其他自身免疫病。与此不同,MOG抗体阳性的患者中只有9%合并其他自身免疫病。系统性红斑狼疮、干燥综合征、重症肌无力在AQP4抗体阳性的NMOSD患者中很常见,在我们的MOG抗体阳性的患者群体中却从未出现过。这与最近一项研究的观点不谋而合,这项研究显示,AQP4抗体血清反应阴性的NMOSD患者合并自身免疫病的概率比较低。有意思的是,某位患者抗甲状腺过氧化物酶抗体、抗甲状腺球蛋白抗体、抗TSH受体抗体相关的甲状腺功能亢进的首发症状仅仅发生在MOG抗体阳性脊髓炎首次发作之后的7周,这说明,MOG自身免疫反应仅仅是本例广泛免疫失调中的一环。 疾病分类 2015的NMOSD诊断标准要求“选择性诊断”需被排除。但是,我们并不清楚MOG抗体阳性的视神经炎或脊髓炎是否应该作为“选择性诊断。AQP-IgG阳性和OG-IgG阳性的EM在靶结构、免疫组织病理学方面是不同的,但是MOG抗体并没有被明确的认定为排除标准。这反映出:诊断标准有所改进,但MOG抗体阳性患者的数据依旧缺乏。 根据目前的研究,所有MOG抗体阳性患者中,只有三分之一符合AQP4抗体阴性NMOSD的临床及影像诊断标准。如果MOG抗体不被视为NMOSD的排除标准,将导致部分MOG抗体阳性的患者被认为是符合NMOSD的临床和治疗标准,另一部分仅仅因为表型不同被排除,尽管所有人都属于同样的疾病谱免疫基因型。这可能会导致相关结论的偏差:几乎所有符合NMOSD诊断标准的患者均曾患ON或LETM,但是根据最终随访,他们中大多数都不符合孤立ON或孤立LETM的诊断标准。同样,将MOG抗体阳性的患者纳入NMOSD人群中也会造成误解。 所以,我们认为确认MOG抗体血清阳性的患者应该作为NMOSD的排除标准,NMOSD应该严格被限定为AQP4抗体阳性的患者或血清中二者均阴性但符合AQP4抗体阴性 NMOSD标准的患者。 这种方法有两种潜在的局限性。第一,若将MOG抗体血清阳性作为NMOSD的排除标准,需要提供MOG抗体测试的参照实验,需要建立多中心模式来保证较高的特异性。或者,可以像最近建立的NMOSD标准一样,建立MOG抗体阳性NMOSD的诊断标准(建立在血清学和支持性的临床标准基础上)。第二,所谓的双阳性患者,也就是MOG抗体及AQP4抗体均阳性的患者,面临着诊断困境。但是,此类患者应该被临床试验排除在外,因为他们可能患有两种独立的疾病。而且,双阳性的患者非常罕见,目前世界范围内已报道的少量案例均没有最终确诊。 局限性 我们承认,我们的研究存在一些明显的局限性。首先,就像该领域所有先前的研究一样,我们的研究设计是回顾性的,并且涉及到了大量的神经中心。然而,因为发病率低,回顾性的单中心研究想要纳入足够多数量的患者是很难实现的。而且,本研究的多中心设计包含了11个学术中心,减少了转诊偏倚,转诊偏倚是作者之前关于NMO的单中心研究中可能存在的局限性。而且,我们最近才研究中检测MOG抗体的可靠方法,所以,目前只有长期的回顾性研究数据是可用的。其次,良性或单相长期病程的患者不太可能被送进医院,所以在目前的人群中患者人数不足。但是,此种类型的潜在误差是以医院为基础的所有研究的固有误差,并不能完全避免。所以,所有涉及到的中心都应有针对神经炎的转科门诊,住院和门诊的患者都应该被纳入进来。在德国和意大利,公共医疗是免费的,所以准入门槛很低。第三,在根据临床及影像学特征被诊断为ADEM的患,尤其是儿童,也曾检测出MOG抗体阳性。这些案例被没有包含在目前的研究人群中,我们纳入的是ON和或脊髓炎的患者。我们的研究发现,大多数MOG抗体阳性的CNS炎症的患者为复发性病程,部分病例在首次发作后数年才会复发,所以,我们需要系统性的后续研究来之前诊断的ADEM与MOG抗体之间的关联。 结论与展望 总之,我们的研究证实,MOG抗体相关的视神经炎和脊髓炎通常为复发性病程,且在大量患者中会导致严重的和或持续性的残疾。视神经损害导致的功能性失明是最常见的后遗症。下肢轻瘫、感觉迟钝和疼痛是脊髓炎患者的常见症状。部分患者只经历了仅仅表现为感觉症状的轻度发作,这些人的核磁上可能看不到病灶也没有电生理的改变。虽然我们的群体中大多数MOG抗体阳性的脊髓炎有LETM,但是非长节段病变并不能排除诊断。端脑、脑干或小脑的临床症状和影像学改变常常是共存的,在一些案例中病变可以十分广泛。脑干症状包括难治性的恶心呕吐和致命的呼吸道并发症。在AQP4抗体阳性的NMOSD中,脑脊液检查表明,大部分患者有轻度的脑脊液细胞数增多,与MS不同,在绝大多数案例中,我们没有发现IgG鞘内合成的证据。在许多患者中,IVMP和PEX治疗是有效的,免疫抑制疗法后,经常可以换来无发作期。但是,我们注意到有几例患者,急性长期治疗是失败的,随后便很快出现了残疾。特别要注意的是,MOG抗体阳性患者在急性发作期中止IVMP治疗后经常会出现爆发性发作。部分患者在PEX治疗后完全恢复,包括对IVMP无效的患者。采用AZA治疗患者的严重发作通常发生于AZA的潜伏期内和未与口服激素联用的患者中。MTX被认为对MOG抗体阳性的视神经炎和或脊髓炎可能有效。干扰素-β仅被用于误诊为经典MS的少量患者,且与疾病活动增加相关。利妥昔单抗对部分患者有效,但是部分患者在首次输注后的几周内就会出现新的发作,与AQP4抗体阳性的NMOSD相似。我们的研究包含了部分最年轻和最高龄的白人MOG抗体阳性患者,这说明,表现为视神经炎或脊髓炎的患者,不限来源,无论年龄,我们都应该考虑MOG抗体阳性的可能。女性比男性更易患病,且病情可能更重。与AQP4抗体阳性的NMOSD相比,MOG抗体阳性的NMOSD共存的自身免疫比较少见。AQP4抗体阳性的NMOSD与经典的MS在临床和影像有大量重叠,所以很多患者最初被诊断为MS。部分MOG抗体阳性的视神经炎和或脊髓炎患者符合2015版NMOSD国际诊断标准,部分是不符合的。假定所有的MOG抗体阳性的患者都具有相同的免疫学机理,从疾病分类学的观点来看,这是有问题的。迄今为止,有些临床和影像的特点是AQP4抗体阳性的NMO的特征,比如:长节段脊髓病灶,病灶位于激素中央部,纵向延伸的视神经病灶,病灶累及视交叉,极后区病灶,难治性恶心呕吐和丘脑病灶;MS的特征表现:INO,室周的,皮质下,皮质旁和胼胝体白质病灶,部分MOG抗体阳性的患者也可能有以上特征。与AQP4抗体阳性的NMOSD和MS相似,部分患者的首次发作或复发是由感染或免疫接种诱发的。在我们研究群体的曾生育的所有女性中,大约有30%的人至少有一次发作发生在孕期或产后。之前的研究(小规模横断面研究,观察期较短)认为,MOG抗体属于一种病情较轻的单相病程的NMOSD,我们的研究(主要针对白人)却否认了这种观点。MOG抗体阳性的视神经炎和脊髓炎常为复发性严重病程,需要考虑长期免疫抑制治疗。对于MOG抗体阳性的EM,前瞻性的多中心研究和实验性治疗是很必要的,但因为罕见的条件而很难操作。
姚要兵 主治医师 郑大一附院 神经内科4825人已读 - 精选 长期应用激素的注意事项
遵医嘱按时按量用药。长期使用糖皮质激素类药物的患者,病情好转后,在医生的指导下缓慢减量,切忌自行停药。突然停药可使原有症状出现或病情加重,称为反跳现象,应逐渐减少用药次数和剂量,直至完全停药。 用药时间:早上6—8点用药。在6—8点使用激素类药物对肾上腺分泌功能的抑制作用比在午夜时用药减小2倍。因为血浆糖皮质激素水平在6—8点时达到峰值,此时血液中糖皮质激素水平上升,对肾上腺分泌促肾上腺糖皮质激素的抑制作用减小。 服用糖皮质激素有胃肠道出血的风险,长期使用激素应常规服用保护胃的药物,能有效预防胃肠道出血;同时应在饭后服药。 激素有引起骨折的风险,长期使用都应常规补钙和维生素D,能有效预防骨质疏松。 部分病人用药后血压血糖会升高,停药后可恢复;治疗早期应在医生的指导下监测血糖、血压,适当的运动、清淡饮食;调整降压药。 长期吃激素抵抗力会变差,容易感冒;而感染是引起病情复发的重要因素,应注意通风保暖,避免过度疲劳,预防感冒,出现症状应积极就诊。 吃了激素会发胖,形成满月脸、水牛背; 但合理的饮食,可以控制体重过度增长,激素减量之后,体型可逐渐恢复。 少数病人治疗中可能出现失眠或情绪异常,如果失眠比较严重,可以在医生的指导下间断使用一些治疗失眠的药物
姚要兵 主治医师 郑大一附院 神经内科3321人已读 - 精选 多发性硬化的健康食谱
multiple sclerosis,MS)患者身上同样适用。虽然每个 MS 患者对健康饮食的反应不尽相同,但营养和均衡饮食对身体健康的重要性是毋庸置疑的,尤其对 MS 患者更是如此。 ” 健康均衡的饮食搭配对身体有如下益处: 1、保持健康体重 2、减少疲乏感 3、维持正常肠道和膀胱功能 4、降低患皮肤病的风险 5、维持骨骼健康强壮 6、维持口腔健康 7、增强心脏功能 8、提升肌肉力量和运动幅度 9、提升灵活度 10、减少某些特定疾病的发生率,比如心脑血管疾病、骨质疏松和某些恶性肿瘤 而如果你打算大幅度地改变饮食习惯,最好先咨询你的医生或专科护士。 改善膳食模式,助你一臂之力 均衡搭配饮食最重要的原则是:不挑食、不偏食,目的是为了保证每一种重要营养物质的每日摄入量。根据《中国居民膳食指南》推荐 [1],平衡膳食模式可最大程度上保障人体营养的需要,也是人体维持健康的基础。而食物多样是平衡膳食模式的基本原则,包括 MS 患者在内的所有人,在选择饮食时应该注意以下几个原则: 01 食物多样,谷类为主 每天的膳食应包括谷薯类、蔬菜水果类、畜禽鱼蛋奶类、大豆坚果类等食物。建议平均每天摄入 12 种以上食物,每周 25 种以上。 02 吃动平衡,健康体重 体重是评价人体营养和健康状况的重要指标,吃和动是保持健康体重的关键。各个年龄段人群都应该坚持天天运动、维持能量平衡、保持健康体重。体重过低和过高均易增加合并症的风险。 03 多吃蔬果、奶类、大豆 蔬菜、水果、奶类和大豆及制品是平衡膳食的重要组成部分,坚果是膳食的有益补充。蔬菜和水果是维生素、矿物质、膳食纤维和植物化学物的重要来源,奶类和大豆类富含钙、优质蛋白质和 B 族维生素,在降低慢性病发病风险方面具有重要作用。 04 适量吃鱼、禽、蛋、瘦肉 鱼、禽、蛋和瘦肉可提供人体所需要的优质蛋白质、维生素 A、B 族维生素等,有些也含有较高的脂肪和胆固醇。动物性食物优选鱼和禽类,鱼和禽类脂肪含量相对较低,鱼类含有较多的不饱和脂肪酸;蛋类各种营养成分齐全;吃畜肉应选择瘦肉,瘦肉脂肪含量较低。 05 少盐少油,控糖限酒 我国多数居民目前食盐、糖分、烹调油和脂肪摄入过多,这是高血压、肥胖和心脑血管疾病等慢性病发病率居高不下的重要因素,因此应当培养清淡饮食习惯,提倡饮用白开水和茶水,不喝或少喝含糖饮料。 均衡膳食模式怎么选,先弄清这几个问题 有道是知易行难,光是知道均衡膳食模式的原则远远不够,还需要一步一步学会如何均衡搭配饮食,一般而言,选择正确的膳食模式,患者需要想清楚以下几个问题: 你的膳食模式有无合理的科学证据支撑? 无论是网上还是朋友之间的讨论,各种膳食模式五花八门。一份好的膳食模式应该有强有力的科学证据作为支撑,普通人如果无法辨别的话,一定要从权威的渠道去获取这些信息,坊间传言可能会不靠谱。 你选择的饮食方式会让你感到煎熬吗?你是否被要求不能再吃你喜欢的食物?因饮食习惯不再一致而不得不拒绝家人朋友间的聚会? 好的膳食模式不应让你长久处于痛苦之中。一下子完全抛弃自己喜欢吃的食物可能导致需求扭曲,从而造成报复性进食。膳食模式的切换应当是循序渐进的,让身体逐渐适应这个过程。而在这个过程中,家人和朋友的支持和理解也非常重要,应当以开放的心态来进行沟通。 你的膳食模式能否为你的生活及健康带来实质性改变? 好的膳食模式对人的影响虽非是立竿见影,但必定是细水长流的。坚持合理膳食必然会对患者的生活带来积极向上的实质性改变。 对你而言,烹饪是棘手的难题吗? 由于 MS 的特性,部分患者可能无法完成一些复杂的烹饪动作,甚至可能带来危险,因此一定要和家人做好沟通,选择合适、方便的饮食模式,比如白灼、清蒸等等。这种简单的烹饪方式实际上也能更好保存食物中的营养,让人吃的更健康。 你选择的膳食模式有得到专业医生或营养师的认可吗? 在进行膳食改进前,患者也需要跟自己的专业医生进行充分的沟通,获得他们的同意后才可以进行。同时,他们的专业观点也能帮助患者弥补原先计划中的不足。 中式食谱推荐 1 早餐 7:30 窝头或馒头:面粉 50 克+玉米面 25 克 蛋丝拌芹菜:芹菜 150 克,鸡蛋 1 个,香油 4 g 脱脂牛奶/豆浆:200 ml 少咸菜、酱豆腐 加餐 10:00 水果 150-200 克 午餐 12:00 米饭:大米 100 克,适当粗粮搭配 香菇油菜:香菇 100 g,油菜 100 g,植物油 4 g 扁豆烧肉:扁豆 100 g,鸡肉 50 g,植物油 4 g 加餐 16:30 原味或无糖酸奶 150 克 晚餐 18:30 花卷:面粉 100 g 茭白烧肉:茭白 150 g,瘦肉 25 g,植物油 4 g 烧圆白菜:豆腐丝 50 g,圆白菜 150 g,植物油 4 g 2 早餐 7:30 杂面发糕:面粉 50 克+黑米面 25 克 鸡蛋 1 个 番茄 100 g 脱脂牛奶/豆浆:250 ml 少咸菜、酱豆腐 加餐 10:00 水果 150-200 克 午餐 12:00 红豆米饭:大米 70 克,红小豆 25 g 炝西蓝花:西蓝花 250 g,植物油 4 g 肉炒胡萝卜丝:胡萝卜 50 g,瘦肉 100 g,植物油 4 g 加餐 16:30 原味或无糖酸奶 150 克 晚餐 18:30 馒头:面粉 100 g 洋葱炒木耳:洋葱 100 g,瘦肉 25 g,木耳 10 g,植物油 4 g 腐竹拌黄瓜:腐竹 10 g,黄瓜 200 g,香油 3 g 3 早餐 7:30 花卷:面粉 70 克 苦瓜拌木耳:苦瓜 50 克,黑木耳 25 g,香油 4 g 煮鸡蛋 1 个 脱脂牛奶/豆浆:250 ml 少咸菜、酱豆腐 加餐 10:00 水果 150-200 克 午餐 12:00 燕麦饭:大米 75 克,燕麦 25 g 肉末茄子:茄子 100 g,瘦肉 25 g,植物油 3 g 清蒸鱼:草鱼 100 g,植物油 4 g 加餐 16:30 原味或无糖酸奶 150 克 晚餐 18:30 发面饼:面粉 100 g 鸡肉炖鲜菇:鲜菇 50 g,鸡肉 100 g,植物油 3 g 炒茼蒿:茼蒿 200 g,植物油 3 g 多发性硬化,更要食之有道
姚要兵 主治医师 郑大一附院 神经内科2180人已读 - 精选 怎样评估颈动脉斑块的风险
脑卒中的病人,约2/3的脑梗塞与颈部动脉狭窄有关。颈部动脉粥样硬化伴狭窄引起大家的重视,于是人们通过颈部超声来作早期的筛查。这样就产生一个误区,一旦查出颈动脉有斑块,便开始觉得危险,担心哪天会突然发生脑卒中,之后往往会辗转多个医院检查,天天提心吊胆。这样就提出一个问题,如何辨别斑块稳定性?颈部动脉狭窄的危险性在哪里? 血管狭窄这一经典的风险因素只是一种表象,斑块破裂才是造成下游栓塞而发病的主要根源。如何筛查出易损斑块,并采用干预性治疗才是预防卒中的关键。其实这里有临床症状、超声及颈部斑块的高分辨MR分析。临床上就是仍旧有TIA发作或脑梗塞,有症状就表明斑块不稳定,它作为一种事后判断,有明显不足;而超声和高分辨MR分析则是一种预先判断,临床意义突出。 1 易损斑块有哪些不同类型? 易损斑块(Vulnerable Plaque)是指那些不稳定和有血栓形成倾向的斑块,主要包括破裂斑块、侵蚀性斑块和部分钙化结节性病变。斑块破裂并不是易损斑块的惟一内容,那些有血栓形成倾向、可能快速进展成为罪犯斑块的粥样病变都属于易损斑块的范畴。主要的标准包括活动性炎症、薄的纤维帽和大的脂质核心、内皮剥脱伴表面血小板聚集、斑块有裂隙或损伤以及严重的狭窄。次要的标准包括表面钙化斑、黄色有光泽的斑块、斑块内出血和正性重构。易损斑块成分主要包括:富脂质坏死核,出血,钙化,纤维帽。 血管动脉硬化斑块有不同的类型,这取决于斑块的组成成分及结构特征。不同类型的斑块有不同的危险程度,不同类型的斑块应该选择不同的治疗方法。 2 颈部超声,如何辨别斑块稳定性? 斑块的B超易损性评估应首先根据超声结果综合分析:斑块的形态学(规则相对稳定,不规则相对不稳定);斑块的声波特征(均质等回声相对稳定,均质低回声不稳定,强回声不一定是硬斑;不规则形、多发点片状钙化斑块,多数为坏死与指质,陈旧性出血混杂的斑块更易损);血管狭窄程度(血流冲击,易致斑块破裂形成血栓)。斑块软硬只是其中一个影响因素,并非是判定的唯一标准。 首先,看形态。 表面光滑、外形规则的斑块一般不容易破裂;而外表不光滑,形状不规则的斑块,即使结构较硬,也容易在血流的冲击下破裂。举例来说,表层纤维帽厚薄不均的斑块,在遭遇血压起伏时,很容易破裂,破裂后斑块内粥样物质释出,容易形成血栓,血栓脱落造成脑动脉主干的栓塞,有可能引起大面积脑梗死,患者病情严重。 其次,看构成。 钙化斑块较硬,常理来说应该较为稳定,但如果斑块形态不规则,也容易破裂。破裂后,细小斑块被冲到颅内血管,形成脑梗死,这种梗死比血栓造成的脑缺血很难通过溶栓等质量手段清除。超声检查斑块内部回声特征是评估斑块易损性(稳定性)的重要证据。通常超声检查对斑块内部回声分为以下类型: 低回声 —— 主要成分为脂质(胆固醇)、陈旧性出血,炎性细胞等。对于检查出此类斑块的患者,特别是血脂异常者(高于正常者)建议降脂治疗。陈旧性出血者重点是控制血压的稳定性。 低至无回声 —— 通常为斑块内新鲜出血。此类患者多数以饮酒、情绪激动、血压升高或不稳定导致斑块内新生血管的破裂或表面纤维帽的断裂有关。 等回声 —— 主要成分为纤维组织增生;此类斑块相对稳定。 强回声 —— 主要成分为钙化。 混合回声 —— 上述各种类型的斑块特征可出现在同一患者、同一或不同斑块内。 另外,斑块所处的位置也很重要。如果斑块处在血管的分支部位,受到的血流冲击力不同,影响其稳定性,也会造成斑块的破裂与血栓的发生。因此,绝不能检查出是软斑块后心情紧张、思想负担重;也决不能发现是硬斑块后就高枕无忧,疏于防范。 3 颈部高分辨MR,如何辨别斑块易损性? 对于动脉管壁成像来说,MR 是首选技术。MRI能评价易损斑块绝大多数特征,如纤维帽破裂溃疡,钙化,斑块内出血,疏松基质,脂质核。技术的成功取决于以下几点: --颈动脉斑块磁共振成像专用线圈可以显著提高颈动脉斑块成像的信噪比和对比度,从而有利于病变的精确显示和诊断分析。 MRI和超声评价易损斑块的优劣比较 易损斑块分析可以通过MRI和超声来完成,二者均为无创、非介入检查,个性化精准定量评估卒中风险,各有优劣,其中MRI特点明显。MRI-PlaqueView提供自动、优化的操作流程,引导帮助用户进行斑块分析。斑块成分,斑块负荷,斑块内出血分析,是分析的主要内容。 几分钟内,即可以完成血管腔、血管壁及内部形态及成分(如软斑块,钙化斑块,斑块内出血)的分析,分析包括面积,厚度,距离以及血管狭窄程度,有利于血管外科医生、神经内外科医生、介入治疗医生、以及心脑血管医生对病人的干预防治。超声是通过回声来间接判断斑块的性质,受检测者的经验影响较大,其优势是简便,快捷!MRI评价更客观些,费用略高,需要应用专门的软件VPD。 4 对于颈动脉狭窄,临床上的常见问题 对于颈动脉狭窄,临床上常见问题,我们却难以回答。 狭窄率只有40%,是否应行支架? 狭窄只有30%,就绝对不选择CEA或CAS?狭窄率90%,必需支架吗?一定需要治疗吗?这个患者适合他汀治疗吗?治疗期间是否会突发意外? 一个阶段的他汀治疗后,斑块的情况确实好转了吗? 这个患者适合放支架吗?术中的风险有多大? 患者双侧颈动脉均有问题,应该先处理哪边?两侧的方案一样吗? 高危未必狭窄 颈动脉狭窄的患者仍会发生缺血性卒中; 管腔无任何狭窄的症状性脑血管病患者中,仍有6-8%的几率发生AS易损斑块; 颈动脉管腔狭窄的症状性脑血管病患者中,超过20%的动脉血管存在易损斑块(斑块内出血和或纤维帽破裂) 颈动脉超声和MRI-PlaqueView VPD 是目前二种有效的检测斑块性状的工具。不同类型的斑块,发生中风的风险不同,选择的治疗方案也不同。 5 发现颈动脉斑块后,如何处理? 如果狭窄在50%以下且没有临床症状,可以用降脂、抗氧化、钙拮抗剂、抗血小板等药物治疗;如果狭窄在50%以上且有症状,或狭窄超过60-70%,不管有无临床症状,都应考虑采用手术方法,包括颈动脉内膜剥脱术或颈动脉支架成形术等。这是2015年对于颅外颈动脉硬化的治疗指南里的规定,但这其中缺少斑块风险个性化评估内容。 不能仅考虑管腔的狭窄率,斑块的性质更重要。当我们诊断为颈动脉斑块时,不要慌张,这并不一定意味着脑梗塞的发作,而需要行进一步判断。颈动脉粥样硬化的危害主要取决于颈动脉的狭窄程度和斑块稳定性,是否需要治疗取决于危害大小,当然我们依然需要重视这个问题。 控制卒中的各项危险因素是最重要的治疗措施。如增加运动、合理饮食、减轻体重、戒烟、不酗酒、控制血压、血糖、血脂等。治疗手段包括有健康管理、药物治疗、手术治疗(颈动脉内膜剥脱术和颈动脉支架成形术)。 健康管理是一种自律! 知行合一!自我认知,自我管理最重要!
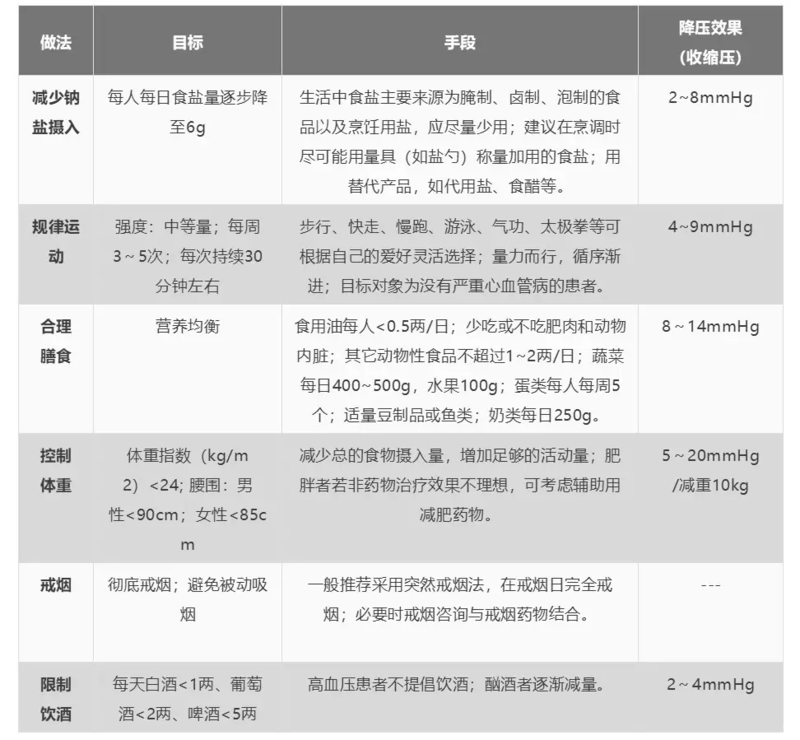
姚要兵 主治医师 郑大一附院 神经内科2368人已读 - 医学科普 降压,降脂,降糖的非药物方法,日常知道大全!饮食疗法!
 姚要兵 主治医师 郑大一附院 神经内科1人已购买
姚要兵 主治医师 郑大一附院 神经内科1人已购买 - 论文精选 多发性硬化最新药物动态及DMT类药物相关知识
多发性硬化(MS)是一种中枢神经系统炎症性脱髓鞘疾病,病情反复,致残率高,给患者和家属带来沉重的心理负担和经济负担。据2018年中华医学会神经病学分会发布的《中国多发性硬化患者生存报告》估计,我国约有3万名MS患者。 疾病修正治疗(DMT)是MS缓解期的标准治疗。近年越来越多国际主流声音支持采用更积极的方式管理MS,及早使用高效DMT药物,以达到无疾病活动证据(NEDA)的治疗目标。 DMT药物在国际上应用已有近三十年时间,但因药物进入中国时间较晚,国内患者对于这类药物的使用仍然存在诸多顾虑,为此针对DMT药物临床应用中的常见问题我们进行了梳理。 Q1 目前有哪些DMT药物可供使用? 目前国际上已批准上市用于MS的DMT药物共有15种,包括干扰素-β1b、醋酸格列默、干扰素-β1a、芬戈莫德、特立氟胺等。 其中,已在国内获批用于MS的DMT药物有注射用干扰素β-1b、口服特立氟胺、口服芬戈莫德和口服西尼莫德,分别于2010年、2018年、2019年和2020年上市。 Q2 现有DMT药物能达到MS治疗目标吗? 近年来,随着医疗水平的进步,国际上越来越倾向针对多发性硬化的“倒金字塔疗法”,即把握黄金治疗窗口,早期使用高效DMT,强有力地延缓疾病进展,减少MS复发和新的MRI活动病灶,满足更高的治疗目标——如疾病活动证据NEDA-4。NEDA-4是指无复发、无残疾进展、无MRI活动和无脑萎缩,其中残疾进展采用扩展残疾状态量表(EDSS)得分变化判断,无MRI活动是指MRI扫描未显示新发或扩大的T2序列或T1钆增强序列的病变,无脑萎缩是指年龄化脑萎缩率
姚要兵 主治医师 郑大一附院 神经内科4人已购买 - 医学科普 患者如何正确使用免疫抑制剂
因病情需要,很多病友们需要服用他克莫司、环孢霉素、吗替麦考酚酯等免疫抑制剂,这些药物浓度过高的话出现毒性的机会大,过低的话治疗作用减少,所以需要将其血药浓度控制在一定范围内。 但是临床诊疗工作中发现有些肾友的血药浓度忽高忽低,或者虽然足量服用,但是血药浓度很低,很显然,他们没有掌握正确的服药方法。因此整理了一些关于免疫抑制剂服用的注意事项跟大家分享一下。 壹 免疫抑制药必须按时服用,如他克莫司、环孢霉素、吗替麦考酚酯需要一天两次的药物,需要间隔12小时服用。他克莫司与食物同服(特别是脂肪含量高的食物),其吸收速率及程度会下降,最好在餐前1小时或餐后2小时服用,以免影响吸收;环孢霉素服药时尽可与牛奶或果汁饮料同服(葡萄、柚汁除外),因为环孢素是亲脂分子,口服吸收慢且不完全,当与某些食物同服时,尤其是脂溶性食物(如牛奶)、果汁或其他饮料同服,会使峰浓度、谷浓度都增高,从而提高其生物利用度;吗替麦考酚酯一般是饭后服用,通常在饭后半个小时比较好,因为可以减小对肠胃的刺激伤害。 贰 如果出现漏服,一定要提高警惕。但也绝对禁止在下一次服药时擅自增加剂量。2次服药间隔时间不应少于8小时,否则可能导致严重的毒副作用。 叁 当必须服用会增加、降低血药浓度的药物时,必须在医生的指导下使用。这些药物包括红霉素、阿奇霉素、苯妥因钠、苯巴比妥、氨茶碱、速尿、酮康唑等。 肆 如果在服用免疫抑制剂后出现呕吐,应按下列方法增加药物用量或者遵医嘱,并注意检测浓度:(1)服药0~10min内呕吐时,加服全量;(2)服药 10~30min内呕吐时,加服1/2量;(3)服药30~60min内呕吐时,加服1/4量;(4)服药60min以后呕吐时,无需加服。 伍 如果在服用免疫抑制剂后出现腹泻,应按下列方法增加药物用量或遵医嘱,并注意检测浓度:(1)水样便每日5~6次,需加服1/2剂量;(2)水样便每日3次,需加服1/4剂量;(3)糊状软便时,无需加服。 陆 某些食品会影响免疫抑制剂的吸收,改变血药浓度。如当他克莫司与食物同服(特别是脂肪含量高的食物),其吸收速率及程度会下降,服用他克莫司时饮酒会增加视觉和神经系统不良反应。环孢霉素和他克莫司与西柚汁同时服用,可以提高两者的血药浓度。 柒 避免使用未经医生同意的药物,包括中药或偏方;药物不同的剂型体内的生物利用度不尽相同,故改换不同的剂型、不同厂家的药物,一定要在医生的指导下进行,以免出现排斥反应或药物中毒。 捌 药品应按说明书保存,避免潮湿、高温或阳光直接暴晒,夏天不要放在未开空调的自驾车里。 玖 建议在服药期间对服药的种类、血药浓度、药物增减、异常症状等进行完整的个人记录。
姚要兵 主治医师 郑大一附院 神经内科1人已购买 - 医学科普 脑脊液寡克隆曲带阳性说明什么问题?
在很多神经系统疾病中, 由于血脑屏障破坏造成血中蛋白质进入脑脊液, 或抗原激发体液免疫反应促进内源性免疫球蛋白合成等原因, 脑脊液中的免疫球蛋白含量往往异常增高,并且在高分辨率的电泳过程中会出现脑脊液寡克隆区带 (oligoclonal bands, OB) ,它是检测中枢神经系统炎性病变鞘内免疫蛋白合成的可靠指标, 具有较高的敏感性和特异性。国外新近研究显示, 脑脊液寡克隆区带是判断鞘内免疫球蛋白合成的金标准, 且定性指标比定量指标的敏感度更高。 提到脑脊液寡克隆电泳这个项目,作为检验人我们应该知道脑脊液寡克隆阳性或阴性结果怎么判读?能为临床提供哪些帮助?与哪些疾病相关? 检测手段 目前,我们用于实验室检测中枢神经内源性合成的手段主要有两种: 1.免疫比浊法计算IgG指数或鞘内IgG合成率,有研究发现使用该方法多发性硬化症患者阳性率31-37%,但是测定IgG、白蛋白存在干扰因素较多,对IgG指数的准确性有一定的影响。 2.免疫固定电泳检出寡克隆条带,提示脑脊液中内源性合成的免疫球蛋白,结果直观,可以明确地判断中枢神经系统内源性合成免疫球蛋白的存在,为临床提供有力的证据。 寡克隆区带阳性的定义 寡克隆区带阳性的定义:血和CSF同时电泳,若CSF中检出而相应的血标本中未能检出寡克隆区带,才能定为阳性。国际上将CSF和血清配对标本IEF结果分5型: 1型-血和脑脊液均无条带,正常脑脊液; 2型 CSF中存在寡克隆区带,血清中未见明显的异常:提示鞘内有IgG合成,见于多发性硬化; 3型-CSF中有寡克隆区带但CSF和血清中同时有另外相同的带,CSF和血清中均有IgG带表明有全身性免疫反应,CSF中又有另外的IgG带,提示也有鞘内合成,见于多发性硬化、SLE及肉瘤病等; 4型-CSF和血清中有相同的寡克隆区带,不提示鞘内有IgG合成,血脑屏障受损,CSF中的区带可能是全身性免疫反应被动扩散入CSF所致,见于格林巴利综合征; 5型-CSF 和血清中有相同的单克隆区带;CSF和血清中都有单克隆带, 来源于CNS之外,见于骨髓瘤、单克隆免疫球蛋白病。 与哪些疾病相关 一、多发性硬化 多发性硬化(multiple sclerosis,MS)是神经科一种常见、以免疫介导攻击中枢神经系统髓鞘为特征的慢性病,以中枢神经系统白质炎性脱髓鞘病变为主要特点的自身免疫病。最常累及的部位为脑室周围白质、视神经、脊髓、脑干和小脑。2018年5月11日,国家卫健委、科技部、工信部、国家药监局、国家中医药局五部门联合下发《关于公布第一批罕见病目录的通知》,多发性硬化已纳入首批国家版罕见病目录。脑脊液检查、诱发电位和磁共振成像三项检查对多发性硬化的诊断具有重要意义。脑脊液检查可为MS临床诊断提供重要证据: 1.CSF单个核细胞数:轻度增高或正常,一般在15×106/L以内,约1/3急性起病或恶化的病例可轻至中度增高,通常不超过50×106/L,超过此值应考虑其他疾病而非MS。约40%MS病例CSF蛋白轻度增高。 2.IgG鞘内合成检测:MS的CSF-IgG增高主要为CNS内合成,是CSF重要的免疫学检查。①CSF-IgG指数:是IgG鞘内合成的定量指标,见于约70%以上MS患者②CSF-IgG寡克隆区带:是IgG鞘内合成的定性指标,OB阳性率可达95%以上。但应同时检测CSF和血清,只有CSF中存在OB而血清缺如才支持MS诊断。 二、格林巴利综合征 格林巴利综合征(GBS)是常见的脊神经和周围神经的脱髓鞘疾病,是以周围神经和神经根的脱髓鞘病变及小血管炎性细胞浸润为病理特点的自身免疫性周围神经病。经典型的GBS称为急性炎症性脱髓鞘性多发性神经病(AIDP)。临床上表现为进行性上升性对称性麻痹、四肢软瘫,以及不同程度的感觉障碍。病人成急性或亚急性临床经过,多数可完全恢复,少数严重者可引起致死性呼吸麻痹和双侧面瘫。脑脊液检查,出现典型的蛋白质增加而细胞数正常,呈“蛋白-细胞分离”现象。早期脑脊液可正常,自第二周起出现蛋白含量增高而细胞数正常,细胞数约在20×10^6/L以下,蛋白早期轻度增加,约60-80mg/dl,第四、五周高达100-1000mg/dl。脑脊液寡克隆:4型 CSF和血清中有相同的寡克隆区带,不提示鞘内有IgG合成,血脑屏障受损,CSF中的区带可能是全身性免疫反应被动扩散入CSF所致。 总之,寡克隆区带在中枢神经系统疾病的检验中具有重要的价值和意义。它是提示中枢神经系统亚急性、慢性炎症病变鞘内免疫球蛋白合成的可靠指标,主要见于多发性硬化症、神经性梅毒、亚急性硬化性全脑炎、脑膜脑炎、视神经炎、急性感染性多神经炎和艾滋病等。
姚要兵 主治医师 郑大一附院 神经内科8人已购买 - 论文精选 脑血管痉挛—中国专家共识
一、 前言 脑血管痉挛 ( cerebral vasospasm )是神经外科的常见临床问题 , 其基础和临床研究是目前国内外神经外科领域内的热点问题之一 , 特别是动脉瘤性蛛网膜下腔出血 ( aneurysmal subarachnoid hemorrhage,SAH ) 致死、致残的重要原因 。目前,aSAH 导致的脑血管痉挛已经引起临床医生的普遍关注 , 但其他原因引起的脑血管痉挛尚未引起临床的足够重视 。 中华医学会神经外科学分 会邀请国内神经外科知名专家经数次讨论达成共识后 , 提出 《脑血管痉挛防治神经外科专家共识 》 ,旨在促进国内神经外科医生对脑血管痉挛有更全面的认识 , 解决脑血管痉挛诊断 、预防和治疗的规范化问题,以造福广大病人 。 二、 脑血管痉挛的定义及流行病学 1. 脑血管痉挛的定义 : 1927 Moniz 首次进行临床病人脑血管造影 , 1937 年 Dandy 首次实施开颅手术夹闭颅内动脉瘤 , 1951 年 Ecker 首次根据脑血管造影作出脑血管痉挛的诊断 。 脑血管痉挛即 “颅内动脉的持续性收缩状态 ” 。 脑血管痉挛的诊断主要根据病人的临床症状体征及脑血管造影的影像 , 如果仅在血管造影时发现血管处于痉挛状态 , 病人没有相应的神经功能缺损症状 , 称为无症状性血管痉挛 ;如果病人出现神经功能缺损症状 , 则称为症状性血管痉挛 , 又称迟发性缺血性神经功能障碍 ( delayedischemic neurological deficit , DIND ) 。 2. 脑血管痉挛的流行病学 : SAH 的发病率在不同国家和地区有差异 , 总体发病率大约为 10 /10 万人/年左右 。 由此推测 。 中国每年大约有超过10 万个新发病例 。 SAH 的最主要病因为颅内动脉瘤破裂 , 约占全部病例的 85% , 这些病例除发病后早期死亡者之外 , 大多数需要手术或介入治疗 。 另有一些病例可能由其他少见原因导致 , 如脑血管畸形 、 中脑周围非动脉瘤性蛛网膜下腔出血 、 硬脑膜动静脉瘘 、脊髓血管性病变 、 烟雾病 、 凝血机制障碍 、 肿瘤性出血、 高血压 、 可卡因滥用等 。 由于诊断方法不同以及地区和人种差异 , 不同的文献中报道的 SAH 后脑血管痉挛发生率差异很大 , 介于 20% ~80% 之间 , 其中症状性脑血管痉挛的发生率大约是 10% ~50% 。 颅脑损伤性 SAH ( tSAH ) 后 , 脑血管痉挛的发生率大约为 27% ~50% , 特别是年轻病 人以及入院时Glasgow 昏迷评分 ( Glasgow Coma Scale, GCS) 较低的病人。 在脑血管疾病介入治疗过程中 , 脑血管痉挛的发生率介于 17%~60% 之间。 神经外科开颅手术,术后也可能出现脑血管痉挛, 发生率在 22%~49%之间 , 如果未能及时诊断和治疗, 可能导致迟发性脑缺血, 严重影响手术疗效。 三、 脑血管痉挛病因 、 病理生理及分类 1.脑血管痉挛的病因 : 位于脑底 Willis 动脉环周围的颅内动脉瘤破裂常导致广 泛 的 蛛 网 膜 下 腔 出血, 流入蛛网膜下腔的血液及其降解产物是导致脑血管痉挛的最主要原因 。 脑血管痉挛的发生率以及严重程度多与蛛网膜下腔积血的多少密切相关。 颅脑损伤、 颅脑手术或血管内介入治疗过程中 ,对血管的损伤、 挤压和牵拉、 血管内操作中的机械刺激、 造影剂等化学物质以及手术中出血流入蛛网膜下腔等因素也可导致脑血管痉挛。 根据文献报道, 一些其他疾病也可能诱发脑血管痉挛 , 如结核性和化脓性脑膜炎 、 偏头痛 、 高血压性脑病 。 2. 脑血管痉挛发生的 病理生理机制 : 根据现有研究成果 , 脑血管痉挛发生的病理生理机制与下列因素有关: (1) 血液及手术器械对血管壁的机械性刺激; (2)血块压迫、 血管壁营养障碍等导致血管壁结构破坏; (3) 氧合血红蛋白氧化成高铁血红蛋白并释放氧自由基造成的损伤 ; (4)各种血管活性物质 , 如 5-HT、 儿茶酚胺 、 血红蛋白及花生四烯酸代谢产物的缩血管作用 ; (5)颅内压增高, 过量脱水治疗而不及时补充血容量; (6)血管壁的炎症和免疫反应。以上各种理化因素均可导致血管壁平滑肌细胞膜通透性改变, 钙离子内流增加 , 同时细胞内钙库释放增多 , 最终导致平滑肌细胞内钙离子浓度增加 , 促使血管平滑肌发生异常收缩, 导致血管痉挛。 因此,钙离子超载是目前公认的血管痉挛发生过程中最重要的环节之一。 脑血管痉挛发生后 , 颅内循环系统出现血流动力学障碍, 导致局部或弥漫性脑血流灌注不足, 脑组织处于缺氧状态, 如果未能及时纠正 , 可能出现一系列临床症状。 因此, 同时注意神经功能的保护有利于改善脑血管痉挛的不良后果 。 3. 脑血管痉挛的分类 : (1) 根据病因 ,可分为 4类 。 ①自发性 aSAH ;②tSAH ;③一些医源性因素 , 如颅脑手术 、 脑血管造影以及血管内介入治疗操作等 ;④较少见的原因 , 如结核性和化脓性脑膜炎 。 (2)根据部位或者范围可分为 3 类 : ①弥漫性脑血管痉挛 ,血管痉挛可同时涉及颈内动脉 、 椎基底动脉 、 大脑中动脉 、 大脑前动脉的近段等多支颅内主要血管 , 造影显示各血管显影不清 , 呈线状 ; ②多节段性脑血管痉挛 , 造影显示一支或数支颅内动脉呈粗细不均的腊肠样或竹节样痉挛 ; ③局灶性脑血管痉挛 , 主要是发生于破裂动脉瘤所在的载瘤动脉的局限性痉挛 。 (3)根据血管造影显示的管腔狭窄程度 , 脑血管痉挛可分为 3 级 : 重度 , 管腔缩窄 50% 或以上 ; 中度 , 管腔缩窄 25% ~50%; 轻度, 管腔缩窄 <25% 。 (4) 根据病程可分为早发性脑血管痉挛和 慢性脑血管痉挛 , 后者也称为迟发性脑血管痉挛。 早发性脑血管痉挛多于出血后 24 小时内发生, 急诊血管造影可发现, 多为破裂动脉瘤附近的单侧局灶性血管痉挛。 传统的脑血管造影通常只能发现颅内 大血管的血管痉挛 ,采用正交极化光谱成像 (orthogonal polarization spectral imaging) 的方法, 可以定性和定 量研究大脑皮层的微循环血流状况。 2003 年一项研究发现, aSAH 后早期 ( 动脉瘤夹闭术前) 有超过 50%的病人发生了节段性的微血管痉挛, 血管直径减少可多达 75%, 由此引起一系列临床症状, 并最终影响临床转归。 因此, 及时发现微血管痉挛的发生并尽早防治 , 是提高脑血管痉挛疗效的关键之一。 典型的迟发性脑血管痉挛多在 SAH 后 第 3~5天开始出现, 第 7~10 天达高峰, 持续 2~3 周后逐渐缓解[12]。 四 、 脑血管痉挛的诊断 1.临床表现: (1) 病史: 明确的颅内动脉瘤破裂导致蛛网膜下腔出血, 病人有典型的剧烈头痛发作史。其他情况还包括颅脑损伤 、 血管内介入治疗、 颅脑手术或其他颅脑疾病史。 (2) 典型症状: 脑血管痉挛本身并无典型的特异性临床表现, 一般在 SAH 后 3~5d, 如果出现意识状态的恶化 , 甚至伴随新出现的局灶定位体征, 如偏瘫、 偏身感觉障碍、 失语, 以及颅内压增高的表现 , 如头痛 、 呕吐等 , 临床除外电解质紊乱 (高钠血症), CT 检查除外继发性脑积水及颅内血肿等后 , 需高度怀疑脑血管痉挛的可能性。 还有不明原因的体温升高、 白细胞上升也需引起临床重视, 存在脑血管痉挛的可能性 2. 临床分级: 对于 aSAH, 临床常用 Hunt andHess 分级和国际神经外科医生联盟 (WFNS) 量表来判断病情严重程度。 3. 辅助检查 : (1) 数字减影血管 造 影 (DSA): 数 字减影脑血管造影是脑血管痉挛诊断的 “金标准”, 对动脉瘤和脑血管畸形的阳性检出率高, 可清晰显示脑血管各级分支。 其缺点是不便在 SAH 后多次重复检查。 在有条件的情况下 , 对怀疑有血管痉挛者可考虑行血管造影 。 如果血管造影证实病人存在严重的脑血管痉挛, 也可以考虑同时行血管内介入治疗,或直接在痉挛部位行血管内球囊扩张术。 (2) 经颅多普勒超声(TCD)血流检测:TCD 是目前检测脑血管痉挛的一种常用方法, 如果 TCD 发现局部脑血管的血流速度增快, 则提示存在血管痉挛导致的血管狭窄 。目前的常用诊断标准为大脑中动脉血 流流速峰值>200cm/s 和(或)平均流速>120cm/s。 这一指标与血管造影显示的严重血管痉挛基本相符。 TCD 的主要优点是无创伤, 可连续多次重复检测 , 可用于动态检测血管痉挛的病程以及评价治疗效果 。 需要注意的是,TCD 检测的特异性较高, 敏感性相对较低 , 其测得数值的准确性与负责检测的 医生的经验和技术有关 ,而且由于颅骨厚度的限制 , 一般只能测定某些特定的颅内血管节段。 在开颅手术中 , 也可利用超声技术在直视下直接检测颅内血管的流速, 了解是否存在脑血管痉挛, 并及时采取针对性治疗措施, 如罂粟碱或尼莫地平局部灌洗等。 (3)CT: CT 对于 12h 之内发生的急性 SAH 的诊断准确率较高 , 根 据 CT 显 示SAH 颅内的部位, 可以间接推测颅内动 脉瘤的部位。但 要注意 SAH 检出率与出血后到接受 CT 检查的时间 、 出血量和部位有关 。 CT 检查距发病时间越长 ,敏感性越低 。 如果出血后 7d 行 CT 检查 , 阳性率下降到仅 50% 左右 。 少量出血可因 CT 层面范围偏差出现假阴性 , 另外对于贫血的病人 (HCT < 30% ) , CT检查也可出现假阴性结果 。 根据 SAH 后 24h 内 CT显示的出血量 , 可推测发生脑血管痉挛的危险性 , 即改良 Fisher 分级 ,下表 。 (4)CTA 、MRA: 目前 CT 和磁共振血管成 像技术日益成熟 。 高分辨率的 CTA、CT 灌注成像能够准确诊断颅内主要血管 , 如颈内动脉、 大脑中动脉、 大脑前动脉 A1 段和基底动脉的严重血管痉挛, 但对于诊断小动脉的血管痉挛, 以及鉴别轻度和中度痉挛, 尚有一定局限性。 五、 脑血管痉挛的防治 1.脑血管痉挛的防治原则: 以下关于脑血管痉挛防 治 的 主 要 循 证 证 据 多 来 自 aSAH 后 的 脑 血 管 痉挛, 其他类型的脑血管痉挛可以此为参考, 根据病人情况酌情处理。 如前所述, 脑血管痉挛一旦发生危害严重, 没有特异性的临床症状和体征, 各种主要辅助检查手段,如 DSA、TCD、CTA 等也都有各自的局限性, 而且脑血管痉挛在临床症状和血管造影的影像上常表现出不一致性。 此外, 迟发性脑血管痉挛多 发生于 SAH后第 3 ~5 天并持续 2 ~3 周 。 因此, 对于脑血管痉挛的防治原则应包括病因治疗 、 预防为主 、 全程治疗 、防治并发症等 4 个方面。 (1) 血管造影或 TCD 提示脑血管痉挛 , 病人有临床症状 : 需要尽早治疗 , 以及动态监测 。 (2) 血管造影或 TCD 提示脑血管痉挛, 病人尚无临床症状 : 建议预防性治疗 , 同时动态监测 ,如出现临床症状, 及时调整治疗方案。 (3)血管造影或TCD 未发现脑血管痉挛, 但病人有临床症状也需要给予治疗, 动态监测 。 (4)对于存在脑血管痉挛高危因素的病人, 如自发性 aSAH、tSAH 及大血管周围手术后等, 尽管病人暂时没有临床症状, 仍需加强病情监测 , 并给予预防性治疗。 (5)具体治疗措施的原则包括改善血液动力学参数、 恢复脑血管自动调节机制 、 维持有效血容量、 保持有效脑灌注、 控制颅内压及预防脑水肿等。 (6)一般性防治措施的两个核心环节是血压和液体( 血容量以及电解质平衡) 的管理。 2.病因治疗: 对于自发性 SAH 的病人, 早期病因治疗是治疗成功的关键。 应在病人就诊后尽早行脑血管造影( 或 CTA) 检查 , 一旦证实为颅内动脉瘤破裂, 视病人情况尽早开颅行动脉瘤颈夹闭手术或血管内栓塞治疗。 这样可以显著减少动脉瘤再次出血危险 , 并为清除引流 SAH 创造条件 , 如病人来院时已超过最佳治疗时机, 则应根据病人病情决定 。早 期 尽 可 能 地 清 除 蛛 网 膜 下 腔 的 积 血 是 预 防SAH 后脑血管痉挛的有效手段。 在对动脉瘤等病因处理后 , 脑脊液引流可清除蛛网膜下腔积血及减少其他致痉物质 , 降低颅内压, 预防脑积水。 常用的方法包括反复腰穿引流血性脑脊液、 脑池或脑室内持续引流、 腰椎穿刺置管持续引流。 在一般的颅脑手术, 以及血管内介入操作中 , 也要考虑尽可能减轻局部血管刺激和损伤 、 避免手术中出血流入蛛网膜下腔, 诱发脑血管痉挛。 3. 药物治疗: (1) 钙拮抗剂 : 通过阻止血管平滑肌细胞的钙异常内流来降低脑血管痉挛的发生率和严重程度 , 是临床防治脑血管痉挛的最常用的方法。国内外多项循证医学研究结果均证实钙拮抗剂能够降低 aSAH 血管痉挛所致的缺血性神经功能损伤 ,减少病人死亡率, 改善预后 。 在各种钙拮抗剂中 , 目前临床推荐使用的主要是尼莫地平 。 这是一种具有颅内血管高度选择性的第二代 二 氢 吡 啶 类 钙 拮 抗剂 , 对于颅内血管以外的 其他血管扩张作用较弱 。2007 年 Cochrane 中心的荟萃分析显示 , 尼莫地平显著减少 aSAH 后继发缺血症状 , 使脑血管痉挛所致的死亡和致残相对危险度均明显下降。 尼莫地平目前也是美国心脏协会(AHA)、 加拿大及意大利 等多个国家和地区的 aSAH 诊疗指南中推荐防治脑血管痉挛的首选药物。 遵循早期 、 全程、 足量、 安全的原则 ,推荐尼莫地平的用法和用量如下 : ①早期 : aSAH 病人入院后应尽早开始给予尼莫地平 , 建议静脉输注。 《J Neurosurg》 的荟萃分析证明 , aSAH患者在发现出血后预防性应用尼莫地平可显著减少脑 血 管 痉 挛 引 起 的 神 经 损 伤 和 死 亡。 2006 年《Neurosurg Rev》 对脑血管痉挛防治的综述表明 , 尼莫地平被用于大多数 aSAH 患者脑血管痉挛的预防性治疗 。 对听神经瘤手术的病人 , 2007 年《Neurosurgery》上发表的随机临 床对照试验表明 , 从开颅术前 1d 开始预防性使用尼莫地平注射液, 预防术后神经功能缺损的疗效显著优于从术中开始使用 。 ②全程: 脑血管痉挛在 aSAH 后可持续 2 ~3 周 , 因此尼莫地平维持治疗至少需 14 ~21d。 《Youmans Neuro -logical Surgery》第 5 版中明确指出 , 处理蛛网膜下腔出血患者脑血管痉挛的一个重要原则是使用尼莫地平, 疗程为 21d[24]。 建议尼莫地平静脉滴注 14d, 后改为口服序贯治疗。 ③足量: 尼莫地平静脉输注的剂量依体重而定 。 体重低于 70kg 或血压不稳的病人: 起始剂量为 0.5mg/h, 如耐受良好, 2h 后可增加至 1mg/h; 体重﹥ 70kg 的病人: 起始剂量为 1mg/h, 如耐受良好, 2h 后可增加至 2mg/h。 每天静脉给药剂量为 24 ~48mg。 尼莫地平半衰期约 1.5h, 静脉给药建议采用输液泵持续给药, 以便保持稳定的血药浓度 。 口服推荐 剂 量 为 60mg, 每 4 h 1 次 。 ④ 安 全 : 2007 年Cochrane 中心荟萃分析结果证明 , 尼莫地平不增加aSAH 后再出血的发生率。 国际大规模临床试验证明尼莫地平对颅内压的影响与安慰剂相似。 ⑤术中局部灌洗: 将新配置的尼莫地平稀释液 (1:19 尼莫地平注射液/林格氏液 ) 加温至与血液温度相同后 , 于术中脑池滴注。 (2) 镁剂:国内外一些临 床研究证实, 硫酸镁对脑血管痉挛有一定的防治作用 。 起始剂量为 10mg/Kg 体重静脉滴注, 维持剂量为 30mg·kg-1· d-1。 目前镁剂防治脑血管痉挛尚未得到其他指南推荐。 (3)罂粟碱:罂粟碱是一种血管扩张剂 , 局部应用可高选择性作用于痉挛动脉, 缺点为作用时间短暂, 对老年病人的血管舒张作用下降。 用法: 0.3%罂粟碱溶液 100 ml 以 0.1 ml/s 速度动脉内灌注。 可用于血管内介入治疗时动脉内灌注或开颅手术中局部灌洗。 具体使用方法请参照药品说明书 。 (4) 其他药物:法舒地尔是一种蛋白激酶抑制剂 , 主要通过抑制 Rho 激酶活性, 减少血管平滑肌细胞对细胞内钙离子浓度增高的敏感性 。 日本一项随机临床试验(275 例 SAH 病人) 证实法舒地尔能减 少脑血管痉挛发生。 根据其使用说明 , 为避免诱发动脉瘤再破裂出血的危险性, 应在导致 SAH 的颅内动脉瘤被夹闭或栓塞后再开始使用 , 而且用药时间不宜超过 2 周 ,其剂型为静脉制剂。 法舒地尔的推荐用法为每日 2 ~3 次, 每次 30 mg 静脉滴注 30 min。 关于内皮素受体拮抗剂的临床试验证实它具有缓解血管痉挛的严重程度 、 降低脑缺血发生率的趋势 。 一些关于卒中的临床试验提示, 他汀类药物也能降低脑血管痉挛的发生率, 改善预后 , 目前尚处于临床试验阶段。 4. 血管内治疗: 脑血管痉挛的血管内治疗有两种常用方法: 球囊血管扩张成形术和动脉内血管扩张药物直接灌注。 二者可单独或联合使用 。 有研究表明 , 对于严重的节段性脑血管痉挛, 球囊血管扩张术后数小时内 , 60% ~ 80% 病人的临床症状有明显改善。 球囊扩张技术的并发症与操作相关 , 包括造成急性动脉夹层、 动脉瘤夹移位等。 一般只适用于颅内大动脉的局限性痉挛。 5.血流动力学治疗: 升高血压 、 扩容和血液稀释合称为 3H 治疗, 是临床较为常用的一种方法。 如果采用 , 必须有加强监护措施 , 即相应的动脉压 、 中心静脉压、 血常规、 生化等动态监测手段。 目前一般采用的具体措施为: (1) 升高动脉压应该在颅内动脉瘤手术或栓塞治疗成功之后开始 , 收缩压可维持在140 ~ 200 mmHg (1 mm Hg=0.133 kPa) 水 平 , 根 据临床症状改善程度加以调整 。 升血压的常用药物为多巴胺, 也可考虑采用多巴酚丁胺或肾上腺素 。 (2)扩 容 治 疗 必 须 监 测 中 心 静 脉 压 , 维 持 在 8 ~10mmHg, 即 100 ~130 cm H2O (1 cm H2O=0.098 kPa)。(3) 血液稀释治疗可选用胶体溶液 , 降低红细胞压积至 30 %~35 %。 在使用 3H 治疗时 , 要注意相应的并发症 , 如升高血压可增加心肌工作负荷 , 导致心肌缺血; 循环容量增加可能导致肺水肿 、 血管源性脑水肿 、 低钠血症, 血液粘稠度下降, 血小板聚集能力减低可能诱发出血等。 禁忌症: 破裂的动脉瘤尚未夹闭或栓塞; CT显示已经出现严重脑梗塞 ; 颅内压明显增高, 合并严重脑水肿 ; 病人合并严重的原发性心肾疾病等。 六、 小结 脑血管痉挛是神经外科的常见问题之一 , 与自发性 SAH、 颅脑损伤、 开颅手术以及血管内介入治疗等密切相关, 应引起广大医师的广泛重视。 早期诊断和尽早采取有效的预防和治疗措施是减少脑血管痉挛的发生、 改善预后的关键环节。 但脑血管痉挛的机制复杂 , 而且一旦发生预后不良 , 病死率、 病残率较高, 临床上应予以充分重视。 本共识仅为专家学术性共识意见 , 实施时仍需根据病人具体的病情而定 , 采取各种预防及治疗措施前应参阅相关产品说明书 。 随着医学的不断进步,本共识内容也将进行相应更新。
姚要兵 主治医师 郑大一附院 神经内科2006人已读 - 医学科普 癫痫患者生活注意事项
1.癫痫病人在日常生活中怎样预防癫痫发作? 对于癫痫患者来说,最可靠的预防就是定时,定量长期规律地服用抗癫痫药物。一旦确诊了癫痫,就要马上开始治疗,预防癫痫的频繁发作。如果延误治疗,癫痫反复发作增加了意外伤害的风险,也可能导致身体和智力的伤害。部分癫痫病人和家属对抗癫痫药物副作用的顾虑大于癫痫发作本身,宁可发作几次也不愿意吃药。相比而言,药物副作用的伤害肯定比反复癫痫发作的伤害要小得多。除了长期规律服药,我们也要预防引起癫痫的诱发因素,如饮酒,疲劳,熬夜,发热,大量饮水,暴饮暴食,情绪剧烈波动等。 2.预防发作引起的意外伤害 在癫痫没有得到良好控制前,癫痫患者应该注意: (1)避免从事危险作业,如:高空作业,水上作业,接触火源、强酸强碱,驾驶等行业。 (2)远离火源,或需家人陪伴。 (3)洗澡或游泳时需家人陪伴。 (4)尽量减少独处的时间,告诉身边的亲友癫痫急救的常识 3.癫痫发作了怎么办? (1)保持镇静,使患者远离火源、尖锐物等危险环境,不要试图通过按压患者身体或者掐人中的方式终止癫痫发作。癫痫发作发作具有一过性,通常在5分钟内自行缓解,不会因为非药物的外力的因素而终止。 (2)在患者癫痫发作时,应解开患者衣扣、裤带,使其保持呼吸畅通,并清除口腔内异物,摘掉假牙,取侧卧位以防口腔异物和分泌物误吸而引起窒息。防止摔伤撞伤。有条件者可给予吸氧等处理。 (3)对持续抽搐超过5分钟者或连续抽搐发作者应紧急拨打120送往附近的急诊室治疗。 4.怀孕期间发作怎么办? 癫痫女性妊娠可能会增加癫痫发作、各种并发症及后代畸形等方面的风险,有必要对癫痫女性进行孕前咨询。患者应该知道母亲服用抗癫痫药,孩子的致畸率比正常人高出2-3倍,不过此类药物也仅仅是一个原因,母亲的身体健康也很重要。应该采取什么办法只发生畸形的机率减低呢? 继续抗痫药治疗:除了少数在计划怀孕前发作已停止多年,辅助检查已没有异常的病人,可在受孕前逐渐减少和停用抗癫痫药外,大多数病人在受孕和妊娠期应继续抗癫痫药物的治疗,因为妊娠期的发作,特别是强直发作,有可能造成母体外伤,导致流产或对胎儿的其它损伤。 简化治疗药物:最好使用单药低剂量治疗,因为目前还没有任何一种抗痫药对胎儿是完全安全的,所以选药的原则仍然是依据病人的发作类型,选择控制发作效果最好的药物。单药治疗可以明显减少胎儿畸形率的发生。补充足量的微生素、无机盐、微量元素和叶酸,保证充足的营养和睡眠,尽量避免服用其它的药物,禁止饮酒。
姚要兵 主治医师 郑大一附院 神经内科暂无购买





